 Идеален газ
Идеален газ
Тук са изведени две класически формули - за налягането и температурата - според кинетичната теория за идеалния газ.
Предпога се, че са известни опитно установените закони на Бойл-Мариот (PV=const при T=const), Гей-Люсак (V=const*T при P=const), Шарл (P=const*T при V=const), както и Уравнението за състоянието на газа (PV=nRT).
Идеалният газ е съставен от неразличми една от друга - тоест еднакви - частици с пренебрежимо малки размери,
между които има значително разстояние.
Тези частици имат еднакви маси, нямат ясна форма (приемат се за сферични),
не взаимодействуват помежду си, освен като удари между тях и са толкова много на брой (числото на Авогадро е около 1023),
че техните средни характеристики са стабилни.
Например посоките в които се движат частиците са случайни и
сборния им вектор на скоростта се смята за нулев:
 [1].
[1].
 Газовете имат обем и маса, но нямат форма - тяхното поведение е едно и също във всякакви съдове.
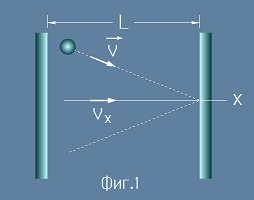
За удобство можем да разгледаме куб със страна L, в който е затворен идеален газ. Частиците на газа се отразяват еластично от стените на куба.
Да приемем, че оста x е насочена перпендикулярно към стената на куба (Фиг.1).
Сумарният импулс, който частиците предават към стените на съда, създава
Газовете имат обем и маса, но нямат форма - тяхното поведение е едно и също във всякакви съдове.
За удобство можем да разгледаме куб със страна L, в който е затворен идеален газ. Частиците на газа се отразяват еластично от стените на куба.
Да приемем, че оста x е насочена перпендикулярно към стената на куба (Фиг.1).
Сумарният импулс, който частиците предават към стените на съда, създава
Налягане
Да означим с vx компонентата на скоростта за една частица. Между два удара
на тази частица върху една и съща стена минава време
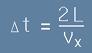 . [2]
. [2]
При всеки удар частицата се отразява и променя импулса си с толкова,
колкото е удвоената му x-компонента:
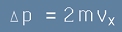 [3].
[3].
Този импулс се предава на стената и по формулата на Нютон F=ma=dp/dt,
това е еквивалентно на действуваща върху стената сила
 [4],
[4],
където индексът 1 на силата F в ляво означава, че това е дял за една частица.
По-горе, в [1] видяхме, че средната скорост на частиците като вектор е нула,
но сбора от квадратите на скоростите не е нулев. Например за всички частици кинетичната енергия е
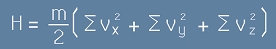 [5],
[5],
където m е масата на една частица а сумата е по отделните частици.
Да означим с N броя на всички частици и да приемем, че средния квадрат на скоростта на една частица е една N-та част от затвореното в скобите на [5]:
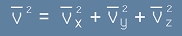 [6] .
[6] .
Тъй като движението е хаотично, трите събираеми от [6] са равни и
за x-направлението се пада една трета:
 [7] .
[7] .
В такъв случай общата сила, която N-те частици от газа упражняват върху стената е
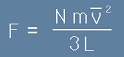 [8] ,
[8] ,
а като вземем предвид, че L2 е площта на стената, получаваме за налягането по формулата P=F/L2
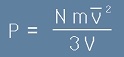 [9] ,
[9] ,
където V от знаменателя е обема на съда; N - брой на всички частици в газа, m е маса на една частица,
a  е средната скорост на една частица,
получена от [6].
е средната скорост на една частица,
получена от [6].
Температура
В уравнението на Клапейрон-Менделеев за състоянието на идеалния газ:
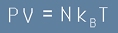 , [10]
, [10]
N е броя на всички частици в газа, P е налягането, T е абсолютната температура, V е обема на газа,
а kB е константата на Болцман.
Да заместим налягането от [9] в [10]:
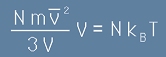 и да умножим това по 3/2. Получаваме
и да умножим това по 3/2. Получаваме
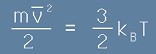 . [11]
. [11]
С думи, средната кинетична енергия на частиците е пропорционална на абсолютната температура.
коментари
Радостин Желязков 23.04.2011
________________________________________________________________________________________
учебни статии по физика
 Идеален газ
Идеален газ
 [1].
[1]. Газовете имат обем и маса, но нямат форма - тяхното поведение е едно и също във всякакви съдове.
За удобство можем да разгледаме куб със страна L, в който е затворен идеален газ. Частиците на газа се отразяват еластично от стените на куба.
Да приемем, че оста x е насочена перпендикулярно към стената на куба (Фиг.1).
Сумарният импулс, който частиците предават към стените на съда, създава
Газовете имат обем и маса, но нямат форма - тяхното поведение е едно и също във всякакви съдове.
За удобство можем да разгледаме куб със страна L, в който е затворен идеален газ. Частиците на газа се отразяват еластично от стените на куба.
Да приемем, че оста x е насочена перпендикулярно към стената на куба (Фиг.1).
Сумарният импулс, който частиците предават към стените на съда, създава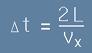 . [2]
. [2]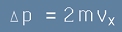 [3].
[3]. [4],
[4],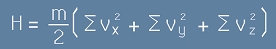 [5],
[5],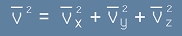 [6] .
[6] . [7] .
[7] .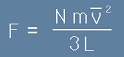 [8] ,
[8] ,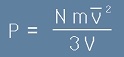 [9] ,
[9] , е средната скорост на една частица,
получена от [6].
е средната скорост на една частица,
получена от [6].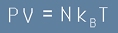 , [10]
, [10]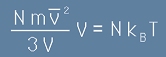 и да умножим това по 3/2. Получаваме
и да умножим това по 3/2. Получаваме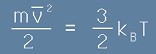 . [11]
. [11]